Gタンパク質シグナルを選択的に活性化し、副作用を抑制し鎮痛効果を向上させた
Advantages
- 副作用低減の作用メカニズム:「Gタンパク質バイアスアゴニスト」として鎮痛シグナルを選択的に活性化するため、動物実験において便秘や呼吸抑制といった副作用の低減が確認されている。
- 経口投与の実現:注射投与が必要な競合薬とは異なり、経口で有効な鎮痛作用を発揮する。
- 高い代謝安定性:ヒト肝ミクロソームを用いた試験で高い安定性を示し、体内での効果持続が期待される。
Background and Technology
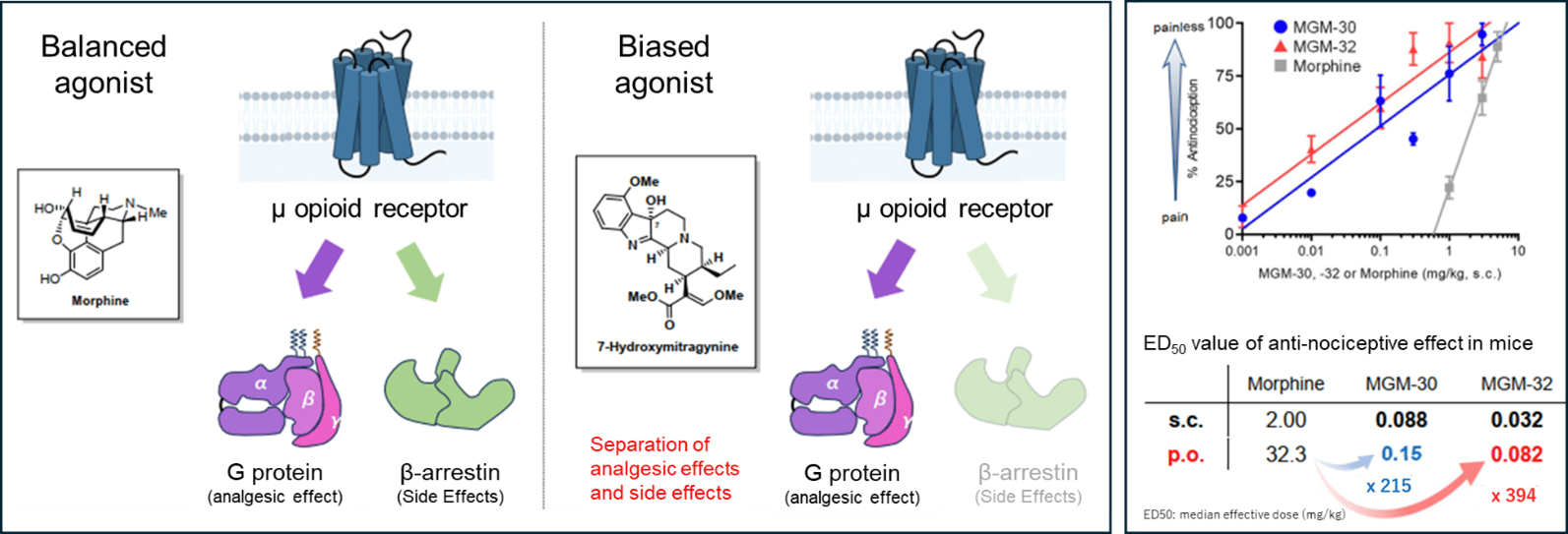
モルヒネに代表される従来のオピオイド鎮痛薬は、強力な鎮痛作用を持つ一方、便秘、呼吸抑制、依存といったβ-アレスチンシグナルが介在する深刻な副作用が臨床上の大きな課題であった。発明者らは東南アジアの薬用植物(Mitragyna speciosa)の活性本体である「7-ヒドロキシミトラガイニン」をリード化合物とした構造活性相関研究を通じて、作用を飛躍的に増強し、代謝安定性を向上させたMGM-30をはじめとする一連の新規化合物を創出した。
Data
- 鎮痛活性:MGM化合物群は、μオピオイド受容体に対して高い結合親和性を示し (MGM-30 Ki値: 0.12 nM)、マウスを用いた試験において、MGM-30はモルヒネの215倍、後続のMGM-32はそれ以上の鎮痛活性が確認された。
- 腸管収縮作用及び呼吸に与える影響:動物実験において鎮痛作用を示す用量域では、既存薬の課題である便秘作用がほとんど観察されなかった。また、呼吸抑制からの回復もモルヒネより速かった。一方で、薬物依存性はモルヒネと同様に認められた。
- 薬物動態およびその他の安全性:MGM-30がヒト肝ミクロソーム中で高い代謝安定性(30分後残存率92%)を示すことが確認された。類縁化合物を用いた初期の毒性試験(Ames試験、hERG試験)では、問題となる結果は得られていない。
Expectations
本研究成果の実用化に向け、製薬企業とのパートナーシップを希望します。特に、大学での実施が困難であるGLP準拠の安全性試験(毒性評価)や詳細な薬物動態試験を共同で推進し、前臨床から臨床開発へとプロジェクトを前進させたいと考えています。また、医薬品製造のためのスケールアップ合成プロセスの共同開発も連携項目の一つです。連携の形態については、共同研究のほか、オプション契約を含むライセンス契約など、企業の開発方針に応じた柔軟な形を想定しています。秘密保持契約下での更なる情報提供が可能です。
Patents
日本:特許第6376702号、米国特許:US 9957262 B2、国際公開番号: WO 2015/064573)
新規化合物(MGM-32)に関する知的財産:特許出願中
Publication
論文:Journal of Medicinal Chemistry (2002: https://doi.org/10.1021/jm010576e), Life Sciences (2004: https://doi.org/10.1016/j.lfs.2003.09.054)
Researchers
高山 弘光_先生、石川 勇人 先生 (千葉大学・大学院薬学研究院)
以下のフォームからお問い合わせください