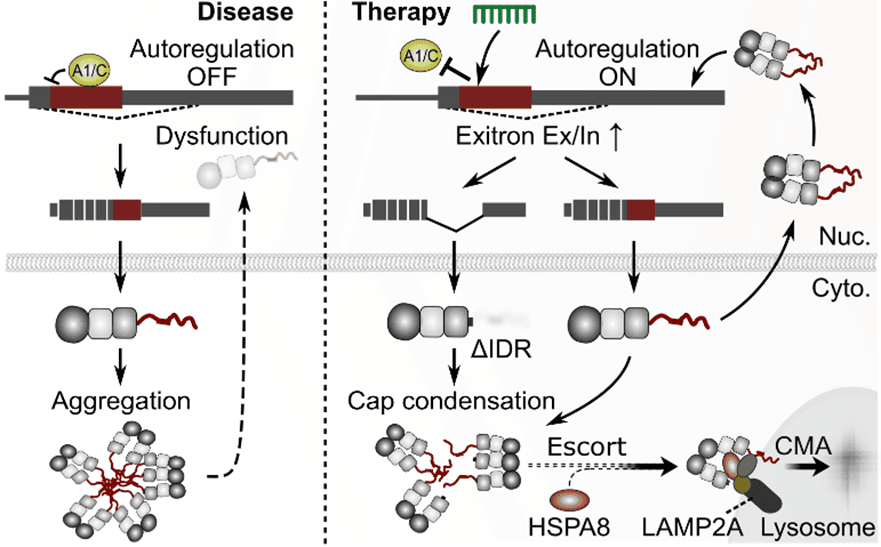
RNA結合タンパクの結合ホットスポットをステリックに遮断するASOで、TDP-43遺伝子内“エキシトロンのスプライシングを再活性化。その結果、凝集の引き金となる天然変性領域(IDR)を作らせにくくすると同時に、保護的な短鎖アイソフォーム(ΔIDR)を増やし、TDP 43凝集をキャップ&エスコート機構で処理へ誘導する。細胞質凝集の抑制と核内機能の回復という二律背反が同時に達成される。
Advantages
- TDP-43病態ループを上流で正す“自己修復”コンセプト:従来の単純な発現抑制や下流補填ではなく、エキシトロンスプライシング制御でIDR負荷低減+ΔIDRによる凝集封じ込めという二層防御を実装。細胞質凝集と核内機能低下の悪循環を断ち切り、TDP 43恒常性を回復させる。
- 孤発性を含む広い適用可能性:TDP 43病理はALS約97%に共通。TDP 43型FTLDにも展開可能な病態横断の標的戦略。
Current Stage & Key Data
疾患モデル動物でのin vivo POCは完了し、GLP試験に向けた前臨床準備期。大学主導で基盤構築を進めており、企業主体による前臨床試験への移行を想定している 。
- TDP-43の凝集抑制と機能回復(In Vitro):ALS様病態(核外漏出と機能低下)を示すヒト神経細胞モデル(siCSE1L)において、HNRNPC結合部位を標的とするASO(CS3)を導入。細胞質TDP-43の異常蓄積を抑制し、核内機能の指標であるSTMN2等の発現/スプライシングを有意に回復。
- ALSモデルマウスにおける治療効果(In Vivo):TDP-43凝集と運動ニューロン変性を呈するALSモデルマウス(Rpt3 CKOマウス)に対し、HNRNPA1結合部位を標的とするASO(AS5)を髄腔内投与。TDP-43異常凝集の抑制と、神経細胞生存の改善に加え、個体レベルで運動機能(握力)の低下を抑制し、生存期間を有意に延長(log rank p="0.011)。
Background and Technology
筋萎縮性側索硬化症(ALS)や前頭側頭葉変性症(FTLD)は、TDP-43の核内機能低下と細胞質凝集が同時に進行するプロテイノパチーである。
TDP‑43は自己制御的にエキシトロン(TARDBPイントロン6由来の隠れエクソン)を切り出し、IDRを含む配列の出力を調整する。病態ではこのスイッチがOFFになり、IDR過多→凝集促進→核内枯渇という悪循環が加速。本ASOはHNRNP A1/C結合をステリックブロックしてエキシトロンスプライシングをONに転換し、
- 層①:IDR負荷の低減(凝集しやすい全長TDP‑43の産生を抑える)
- 層②:ΔIDRアイソフォームの誘導(凝集をキャップし、HSPA8–LAMP2Aを介したCMAでエスコート(分解促進))
という二層機構でTDP‑43恒常性を回復させる。遺伝型を問わず病態の根幹に介入できる点が強み。
Expectations
大学が保有するPOCデータと特許ポートフォリオを基盤に、共同研究開発またはライセンス契約を想定。パートナー企業にGLP試験以降を主導いただき、大学は作用機序・病態評価・バイオマーカーで科学支援する。段階的技術移転によりリスクとタイムラインを最適化。
Patents & Publications
WO2022/113799、WO2023/204313他、複数特許出願中(未公開)
作用機序・有効性データはプレプリント/学会発表で公開済み範囲に基づく記載
Researchers
須貝 章弘 特任准教授 (新潟大学 脳研究所)
以下のフォームからお問い合わせください