細胞内脂質輸送異常を改善するセラミドキナーゼ阻害剤
Advantages
- 新規の作用機序:C1P生成阻害剤は、コレステロールの細胞内輸送異常を改善することで、従来の治療薬が機能しなかった脂質輸送異常を改善する機序であり、新たな治療選択肢となる可能性がある
- 治療選択肢が広がる:既存のニーマン・ピック病C型(NPC)であるミグルスタットとの併用や、同薬の用量低減による副作用軽減にも貢献することが期待される
- 幅広い応用性:NPC以外のライソゾーム病や細胞内脂質輸送異常を伴う疾患にも適用が期待される
Background and Technology
ニーマン・ピック病C型(NPC)は、細胞内の脂質輸送異常によりコレステロールやスフィンゴ脂質が蓄積し、中枢神経症状や精神症状を引き起こす遺伝性の希少疾患である。現在、神経毒性の強いグルコシルセラミドの生合成経路に作用するミグルスタットが治療薬として承認されているが、ライソゾームにおけるコレステロールの異常蓄積には効果がなく、副作用も強いという課題がある。
発明者らは、NPC患者由来の細胞においてセラミド-1-リン酸(C1P)濃度が亢進していることを発見し、C1P生合成に作用するセラミドキナーゼ阻害剤(NVP-231)がコレステロールの脂質輸送の機能不全を改善することを見出した。既存のNPC治療薬とは異なる作用機序により、細胞内脂質輸送異常を直接改善するため、NPCの根本的な治療につながることが期待される。また、セラミドキナーゼのノックアウトはマウスの生存に影響を与えていないことから、治療標的としての安全性も高いと考えられる。さらに、NPC以外にもライソゾーム病に分類される疾患群では、細胞内物質輸送異常(特に脂質輸送異常)が見られることが知られており、これらの疾患に対しての適用も期待される。
Data
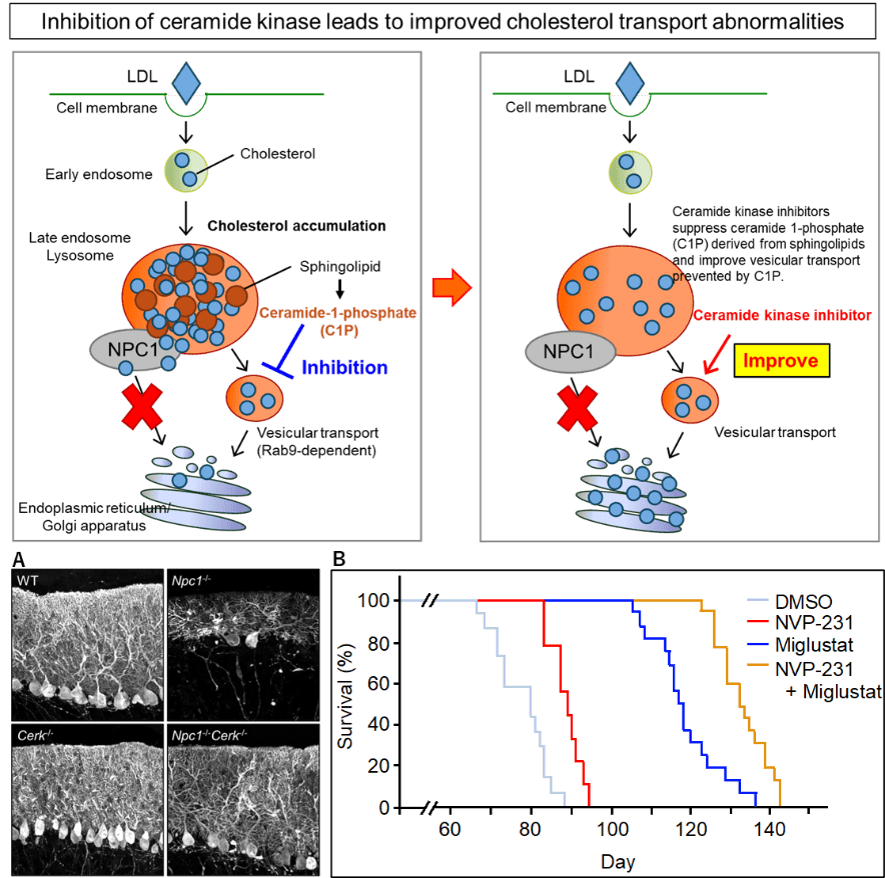
- NPC細胞にセラミドキナーゼ阻害剤であるNVP-231を作用させたところ、後期エンドソームからゴルジ体への小胞輸送の異常が改善し、遊離型コレステロールの蓄積が軽減することを確認した。
- NPCマウスのセラミドキナーゼ(Cerk)を遺伝的に欠損させたダブルノックアウトマウス(NPC/Cerk DKO)において、神経脱落の抑制(A)と生存期間の延長を確認した。
- NPCマウスにNVP-231を投与したところ、生存期間の延長が認められ、ミグルスタットとの併用によってさらに延長効果が認められた(B)。
Expectations
Current Stage
- セラミドキナーゼ阻害薬としてスクリーニングの結果ヒット化合物を取得。誘導体展開によって有効濃度の高い化合物を取得した。
Future Research Plans
- 誘導体のさらなる構造最適化
- NPCモデルマウスを用いた薬効薬理試験
- セラミドキナーゼ阻害剤の薬物動態試験及び安全性試験
Patents
特許第6984854号
Researchers
中村 浩之 教授 (千葉大学)
以下のフォームからお問い合わせください