炎症環境に応答する人工受容体”synNotch”システムによって微小環境を改善する
Advantages
- 炎症環境に応答する人工受容体システムを用いて病変部位特異的に細胞に遺伝子発現を誘導する
- 腸炎モデルマウスを用いたin vivo実験において、潰瘍部位にて炎症抑制因子や増殖因子の産生が可能
Background and Technology
近年の幹細胞研究の進展により、生体外で臓器の一部を再現するオルガノイド培養が開発され、幹細胞やオルガノイドの移植による再生医療が期待されている。しかし、慢性的な炎症により組織再生に重要な微小環境ニッチが失われた病変組織の再生は難しい。また、組織再生のために、強力な抗炎症因子や増殖因子を投与することは健常組織への副作用が懸念される。炎症性腸疾患では、抗炎症薬などで炎症をある程度抑えられても難治性の潰瘍が形成されて上皮が再生されず、大腸全摘出以外の治療法がない患者も存在する。
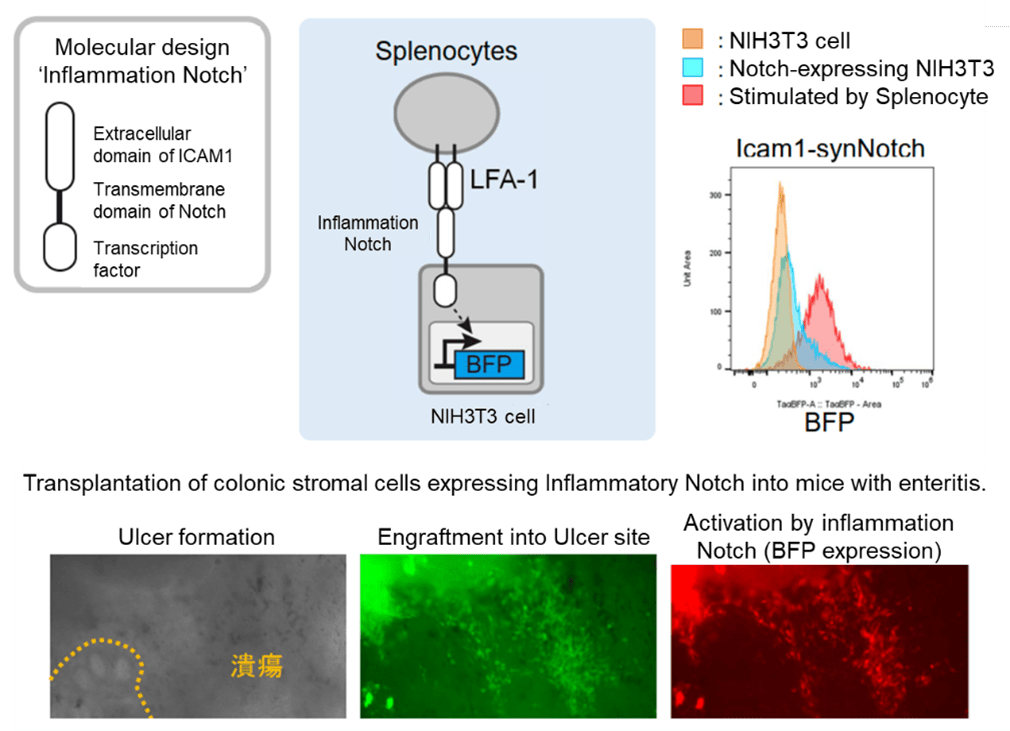
このような状況を改善するため、本発明者は炎症性腸疾患をモデル疾患として、病変部位特異的にニッチを再建する「デザイナーニッチ細胞」を作製した。この細胞は、人工受容体システムsynthetic Notch receptor (synNotch)を利用して炎症や潰瘍などの組織環境変化を認識し、それに応じて抗炎症因子や増殖因子を産生する。実際にin vitro培養系や腸炎モデルマウスを用いた検証により、腸上皮組織の成長誘導や潰瘍部位への生着も確認された。この技術は炎症性腸疾患などの難治性炎症性疾患に対する細胞医薬開発の基盤技術となることが期待される。
Data
- in vitro培養系におけるデザイナーニッチ細胞による腸上皮組織の成長誘導・抗炎症因子の産生を検証
ニッチ因子存在下で成長する腸オルガノイドやLPSに応答するマクロファージを用いて病変組織をモデル化した。まず、GFP(緑色蛍光分子)を分泌する腸オルガノイドとGFPを認識してニッチ因子を産生するデザイナーニッチ細胞を共培養したところ、腸オルガノイド近傍のデザイナーニッチ細胞が活性化した。ニッチ因子が存在しない培養条件下でも、デザイナーニッチ細胞がニッチ因子を産生して腸オルガノイドの成長を促進することを確認した。加えて、炎症細胞を認識して抗炎症因子を産生するデザイナーニッチ細胞を作製し、デザイナーニッチ細胞が産生する抗炎症因子が、LPS刺激によるマクロファージの炎症性サイトカイン産生を抑制することを確認した。 - 腸炎モデルマウスでの検証
大腸由来間質細胞を原料として、炎症細胞を認識して活性化する人工受容体を導入したデザイナーニッチ細胞を作製し、DSS投与により結腸に潰瘍を形成した腸炎モデルマウスの腸内腔に移植した。その結果、デザイナーニッチ細胞は潰瘍部位に生着し、炎症細胞に反応して受容体が活性化して蛍光レポーターの発現を誘導した。さらに移植後5日以上潰瘍部位に留まることを確認し、潰瘍部位にて抗炎症因子や増殖因子を産生できることが示唆された。
Expectations
大阪大学では、本技術を用いて炎症性大腸炎の細胞治療の開発をしていただけるパートナー企業を探しています。発明者との面談による打合せも可能です。
Patents
特許出願中(未公開)
Researchers
戸田 聡 先生 (大阪大学 蛋白質研究所)
以下のフォームからお問い合わせください