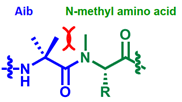
マイクロフロー合成により、いずれも嵩高いAibとN-メチルアミノ酸が隣接したペプチドを合成する方法。
Advantages
- 従来法では立体障害により合成困難だったペプチドを合成できる。
- 安価な試薬のみで短時間で高収率。
- 過剰量の試薬・基質は不要。
- このようなペプチドは医薬品として薬効・経口投与・細胞膜透過性・代謝安定性が期待できる。
Current Stage and Key Data
- 様々な基質でジペプチド合成し高収率を確認済。

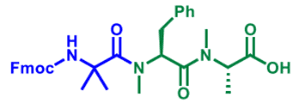
- 得られたジペプチドをそのままペプチド鎖伸長することも可能。
Background and Technology
アミド結合の窒素上に置換基(例えばメチル基)を有するN-置換アミドは、高い生体適合性、細胞膜透過性、及び分解酵素耐性を有し得ることから、薬剤候補分子として注目されている(例:臨床試験中のLUNA18)。
ペプチド合成では一般的に保護アミノ酸の縮合と脱保護工程を繰り返すため、合成労力・時間・廃棄物量の増大を招いている。そのため、遊離のアミノ酸を連続的に連結していく手法の開発が重要と考えられている。N-置換アミノ酸等の嵩高い遊離アミノ酸を連続的に連結してペプチドを合成できれば理想的である。しかしながら、既報告の嵩高いC末端に嵩高いN-置換アミノ酸を反応させて嵩高いアミド結合を伸長する方法は、高価な試薬・過剰な基質・毒性のある試薬・長時間反応・低収率などの理由で産業応用が難しかった。
Expectations
本合成法を用いたペプチド医薬品や農薬の共同開発パートナー、および本合成法のライセンスパートナーを募集中。
- パートナー候補例:ペプチド医薬を開発するバイオテック/製薬企業のCMC部門、ペプチド農薬企業、ペプチド医薬・農薬のCMO/CDMO、フロー合成に注力する化学系企業
Publication
論文:未発表、特許:出願済(未公開)※CDA下で追加情報を開示可能
Researchers
布施新一郎 教授(東海国立大学機構 名古屋大学 大学院創薬科学研究科)
以下のフォームからお問い合わせください