TDP-43病理を呈するALS(筋萎縮性側索硬化症)患者において見出されたmGluR5の機能阻害は、
ALSに対する新たな治療戦略として期待される
Advantages
- 患者由来中枢神経組織から得られた新規エビデンス:ALS患者の大脳運動野および脊髄病変組織を用いて単一細胞核RNAシーケンス解析を実施し、mGluR5の発現増加を新たに同定
- 独自性の高い解析手法:中枢神経組織試料を用いた患者起源データの単一細胞核レベル解析は、試料入手や技術的難易度の点から国内外でも稀少であり、mGluR5発現の異常増加を科学的に実証した独自性の高い成果
- 脊髄運動神経での特異的発現増加:ALS病態の中核である脊髄運動神経でmGluR5発現が顕著に上昇、ALSの運動神経障害に関与する可能性が示唆される
- mGluR5の阻害による神経保護効果:ALS病態モデル細胞でmGluR5発現を抑制すると、神経突起伸長障害が改善
Background and Technology
ALSは、上位および下位運動神経の変性を特徴とする神経変性疾患で、筋力低下や筋萎縮を引き起こす原因不明の難病です。現在も根本的な治療法は確立されていません。ALS患者の約97%に確認されるTDP-43タンパク質の異常蓄積は、運動神経変性と密接に関与していることが知られています。
ALSにおける運動神経障害の発症機構には、cell-autonomous(細胞自律的)機構とnon-cell-autonomous(非細胞自律的)機構の双方が関与すると考えられています。前者は、TDP-43の機能異常やRNA代謝異常など、運動神経自体の内因的な異常によって細胞死が引き起こされる過程を指します。一方、後者は、アストロサイトやミクログリアなどのグリア細胞、あるいは血管内皮細胞の異常が神経細胞機能を障害し、二次的に運動神経障害を誘導する機構を指します。
このように、ALS病態は単一の細胞種に限定された現象ではなく、複数の細胞間相互作用による複合的な障害であると考えられています。その詳細な分子メカニズムはいまだ十分に解明されていないことから、運動神経と周囲の細胞の双方の変化を捉える解析、すなわち本研究のようなアプローチが、病態の本質的理解および新たな治療標的の探索において重要と期待されます。
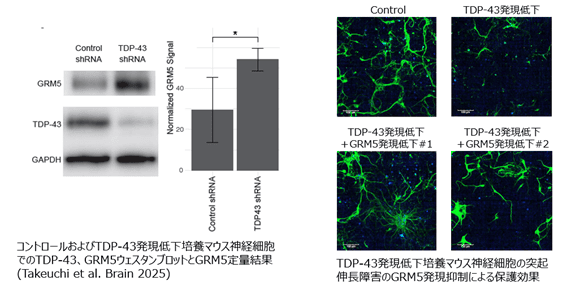
本研究では、TDP-43病理を示すALS患者組織を解析し、グルタミン酸代謝型受容体(mGluR5)の発現が著しく増加していることを発見しました。さらに、TDP-43の発現低下を誘導した培養マウス神経細胞では神経突起の著しい短縮が観察され、mGluR5の発現を抑えることでこの異常が改善されることを確認しました。
これらの結果から、mGluR5はALS病態形成において重要な役割を果たし、その阻害が治療的意義を持つことが示唆されます。また、mGluR5は主に中枢神経系に発現するため、その機能抑制による全身的副作用リスクが低い点も臨床応用上の利点となることが期待されます。
Data
- TDP-43発現をshRNAにより低下させた培養マウス神経細胞では神経突起が極端に短縮。
- 同細胞においてmGluR5をshRNAで抑制すると神経突起伸長が回復し、神経保護作用が確認された。
Expectations
大阪大学では、本発明のライセンス導入またはコラボレーションを通じて、mGluR5を標的とするALS治療薬の開発をご検討いただける製薬企業を募集しています。
次のステップとして、研究者とのご面談をご提案いたします。秘密保持契約を締結しての詳細なご相談やご面談のご希望がございましたらお気軽にお問い合わせください。
Patents
特許出願中(未公開)
Publication
- in vivoモデルを用いたmGluR5機能阻害による治療効果の検証
- 既知mGluR5阻害薬を含む候補化合物のスクリーニングおよび治療効果検証
- 新規mGluR5阻害剤の探索・開発
Researchers
長野 清一 特任教授 (大阪大学大学院連合小児発達学研究科 神経発達・変性疾患共同研究講座)
以下のフォームからお問い合わせください